原子核と放射線
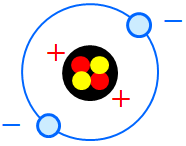
原子は原子核と、その周囲を取り巻く電子で構成されている。電子は負電荷を持ち、原子核には正電荷を持つ陽子と、電荷を持たない中性子が含まれる。陽子と中性子は合わせて核子と呼ばれ、核子どうしを引きつけている力を核力という。
原子核

大きさ
原子の大きさはおよそ10-10mで、原子核の大きさはおよそ10-14m。野球場とボール以上の差がある。
質量
続いて陽子・中性子・電子の質量を比較すると、陽子と中性子にはほとんど差がないが、電子はそれらの約1/1840しかない。よって、「原子の質量」を考えたとき、電子の質量はほとんど考慮しなくてもよい。また、原子の大きさを踏まえると、原子の質量のほとんどが非常に小さな原子核に集中していることが分かる。
| 質量 | 質量比 | |
| 陽子 | 1.673×10-27 kg | 1 |
| 中性子 | 1.675×10-27 kg | 1 |
| 電子 | 9.109×10-31 kg | 1/1840 |

原子の種類は陽子の数で決まり、これを原子番号という(Z)。また、陽子と中性子の数の和を質量数という(A)。このことから、元素Xの原子核に含まれる中性子の数Nは、
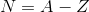
と表されることが分かる。
(例)ヘリウムHe

原子番号Z=2、質量数A=4より、中性子の数Nは4-2=2〔個〕。
ところで、原子の質量は非常に小さく扱いにくい。そこで、質量数12の炭素原子1個の質量数の1/12を1u(ユー)と定めた統一原子質量単位が用いられる。
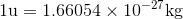
また、原子の中には原子番号Zが等しく質量数Aが異なるものも存在する。例えば、
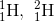
などがあり、これらを「互いに同位体である」という。各同位体について、その存在比に応じて平均した質量を原子量という。
(例)塩素Cl
| 質量 | 存在比 | |
| 35Cl | 34.97u | 75.76% |
| 37Cl | 36.97u | 24.24% |
表より塩素の原子量は、
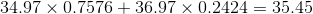
放射線
同位体の中には不安定なものもあり、そのような原子は放射線を出して姿を変える。このような変化を放射性崩壊といい、このような同位体を放射性同位体(ラジオアイソトープ)という。
放射線には複数の種類があり、透過力および電離作用(原子をイオンにするはたらき)の強さによって以下のように分類することができる。
|
|
|
透過力 |
電離作用 |
|
α線 |
ヘリウムの原子核 |
小 |
大 |
|
β線 |
電子 |
中 |
中 |
|
γ線 |
電磁波の一種 |
大 |
小 |
α線は大きいので、紙一枚で防ぐことができるほど透過力が小さい。ところが電離作用が大きいので、体内に取り込んでしまうとさまざまな影響があると言われている。逆にγ線の透過力はとても大きく、これを防ぐには分厚い鉛の板が必要である。ただし、電離作用は小さい。
α線を出す放射性崩壊をα崩壊という。α線の正体は2つの陽子と2つの中性子を持つヘリウムの原子核なので、α崩壊後の原子は質量数が4つ, 原子番号が2つ小さくなる。
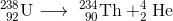
β線を出す放射性崩壊をβ崩壊という。β崩壊では、原子核中の中性子が陽子と電子に変化し、電子が飛び出す。よってβ崩壊後の原子の質量数は変化せず, 原子番号が1つ大きくなる。
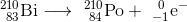
γ線を出す放射性崩壊をγ崩壊という。γ線は電磁波なので、γ崩壊後の原子は質量数も原子番号も変化しない。
半減期
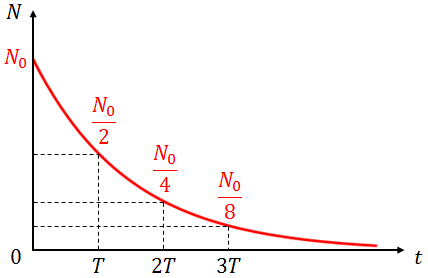
未崩壊な放射性核種の数は、時間が経つにつれて減少していく。このとき、元の核種の数が1/2になるまでの時間を半減期という。元の核種の数をN(0),半減期をTとすると、T→2T→3Tと時間が経過するごとに、



と数が減っていくので、時間tが経過した後の放射性核種の数Nは、
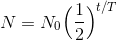
と表すことができる。
以下に半減期の例を示す。
| 核種 | 半減期T |
| ヨウ素131(131I) | 8日 |
| セシウム137(137Cs) | 30年 |
| プルトニウム239(239Pu) | 24000年 |
